- Хто запропонував планетарну модель атома: Історія та значення
- Шлях до творчого прориву: Ернест Резерфорд і його експерименти
- Біографічні нотатки
- Експеримент Резерфорда: Витоки та результати
- Планетарна модель атома: Концепція та структура
- Ключові характеристики планетарної моделі атома
- Значення та вплив відкриття Резерфорда
- Квантова механіка та ядерна фізика
- Далі вдосконалення
- Сучасні уявлення про атом та спадщина Резерфорда
Хто запропонував планетарну модель атома: Історія та значення
Одним з ключових етапів у розвитку сучасної фізики стало відкриття, яке відзначило нового етапу в розумінні будови атома: хто запропонував планетарну модель атома. Цей піонер атомної теорії — Ернест Резерфорд, якому вдалося перетворити основи хімії і фізики, створивши фундамент для подальших досліджень в царині ядерної фізики і квантової механіки.
Шлях до творчого прориву: Ернест Резерфорд і його експерименти
Щоб зрозуміти, якова була дорога, що привела до відкриття планетарної моделі атома, варто заглибитися в життєвий шлях Ернеста Резерфорда та його експерименти, котрі призвели до цього значущого відкриття.
Біографічні нотатки
Ернест Резерфорд народився 30 серпня 1871 року в сільській Новій Зеландії, в родині фермерів. Його кар’єра почалася в коледжі Кентербері, після чого він розвинув свої навички в Кембриджському університеті. Вже на початку своєї діяльності Резерфорд проявив зацікавленість до електромагнітних явищ і радіоактивності, що стали основою його подальших досліджень.
Експеримент Резерфорда: Витоки та результати
У 1909 році, займаючись вивченням розсіювання альфа-частинок, Резерфорд здійснив разом зі своїми учнями Гайгером і Марсденом експеримент, котрий увійшов в історію як “золотий фольговий експеримент”.
- Ціль експерименту: Дослідити поведінку альфа-частинок при проходженні через тонкі шари металу.
- Основні спостереження: Більшість частинок проходили через фольгу без відхилення, проте невелика частина відхилялася на значний кут, а ще менша частка поверталася у зворотньому напрямку.
- Пояснення: Це дало підстави припускати, що атом містить дуже маленьке центральне ядро з позитивним зарядом, достатньо щільне, щоб змусити альфа-частинку змінити свій шлях.
Планетарна модель атома: Концепція та структура
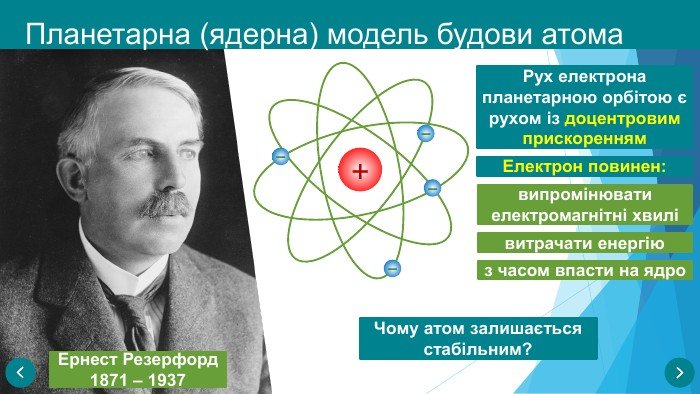
Згідно з концепцією Ернеста Резерфорда, атом нагадує мініатюрну планетарну систему, де електрони рухаються навколо позитивно зарядженого ядра, подібні планетам угорті сонця.
Ключові характеристики планетарної моделі атома
- Центральне ядро: Ядро займає вкрай малий об’єм в атомі, але містить майже всю його масу.
- Електронна оболонка: Електрони обертаються навколо ядра по встановлених орбітах.
- Електростатичне тяжіння: Заряд ядра позитивний і притягує негативно заряджені електрони, що утримує їх в атомі.
Резерфордова модель стала справжнім проривом, надаючи тодішній науці більш чітке бачення структури матерії.
Значення та вплив відкриття Резерфорда
Резерфордова модель атома не тільки спричинила революцію в науці про будову матерії, але й стала фундаментом для наступних відкриттів. Вона не лише пояснила ряд явищ, які до цього не могли бути зрозумілі, але й дала поштовх для майбутніх досліджень у фізиці елементарних частинок і квантовій механіці.
Квантова механіка та ядерна фізика
Хвильова механіка Нільса Бора та інших учених розвивалася на основі концепції Резерфорда, приводячи до розвитку теорії “квантових стрибків” та інших революційно нових ідей. Було розв’язане питання, як електрони утримуються навколо ядра, без втрат енергії у вигляді випромінювання, як це передбачала класична електромагнітна теорія.
Далі вдосконалення
Згодом цю модель було заповнено новими елементами завдяки розвитку квантової механіки. Нові відкриття дали змогу описати атом ще детальніше, висунути концепцію енергій та рівнів електронних обляг, а також структури кори енергії.
| Рік | Відкриття чи вдосконалення | Вклад у розвиток атомної теорії |
|---|---|---|
| 1909 | Золотий фольговий експеримент | Підтвердження існування централізованого ядра |
| 1911 | Публікація планетарної моделі атома Резерфордом | Заміна моделі “пудингової кулі” на сучасне уявлення про атомную структуру |
| 1922 | Вдосконалення Бором хвильової теорії | Введення понять орбіт і підрівнів |
Сучасні уявлення про атом та спадщина Резерфорда
Сьогодні, завдяки еволюції рентгеноструктурного аналізу, синхротронної радіації та комп’ютерного моделювання, наше розуміння атомів зазнало значного прогресу, однак основою завжди залишаються головні принципи, які встановив Ернест Резерфорд.
Сучасна наука продовжує удосконалюватися, відкриваються нові частинки і сили, але основні уявлення, хто запропонував планетарну модель атома, залишаються одними з найбільш вагомих в історії фізики.
Внесок Ернеста Резерфорда в науку важко переоцінити. Його відкриття стало ключовим етапом на шляху до сучасного розуміння атома, зв’язків у молекулах та основних закономірностей фізико-хімічних процесів.